可重构的编码非相干光片阵列实现并行荧光体成
2020-03-09 14:13
可重构的编码非相干光片阵列实现并行荧光体成像
近日,香港大学研究团队用一对接近平行且高反射的平面镜所构成的“无穷镜”实现可重构的非相干光光片阵列。通过编码调制单元,对每片光片加载特定的调制频率,实现对照明光编码,二维图像传感器获取的荧光图像序列包含样品的三维信息,对荧光数据解码即可实现三维荧光成像。所研制的显微镜具有无扫描以及非相干光照明等特点,在器官三维结构、发育生物学、植物生理等需要低损伤的领域具有广泛的应用前景。相关成果于近日以“Parallelized volumetric fluorescence microscopy with reconfigurable coded incoherent light-sheet array”在线发表在国际顶尖光学期刊《Light: Science & Applications》上。
生物体系复杂系统的动态观测仍依赖于光学显微镜。为适应不同研究体系,光学显微镜的两个不同的研究方向是如何提高分辨率以及增大视场范围。以突破光学衍射极限为目的的超高分辨率显微技术,如受激损耗荧光显微术、光敏定位显微术等,获得2014年诺贝尔化学奖。此外,光片荧光显微镜以大视场、多尺度、以及低损伤等优势,在发育生物学、细胞生物学以及组织三维成像等研究中发挥着独特的作用。光片荧光显微镜的一个重要特色就是采用片状的照明光照射样品的特定层,采用侧向宽场成像收集荧光信号,和传统的共聚焦显微镜相比,片状光照明所造成的光损伤更小。为实现三维成像,需要对照明光或者样品进行机械扫描,这限制了三维成像的速度并对系统的稳定性造成一定影响。目前国际上有些报道采用空间光调制器或者简单的机械分光(如分束成3束)将激光束整形成少数片并同时照射到样品上实现并行激发。通过少数片光照明是通向多片并行化迈出的重要一步,然而,由于所生成的光片数目比较少,三维连续成像仍需要借助于机械扫描。此外,由于现有技术采用相干光,在散射介质成像中具有一定的制约,如穿透深度增大后散斑效应强烈。如何有效地采用多片照明并对散射介质中的结构进行低损伤、高时空分辨率成像仍是光学成像领域的一个研究热点。
在这项工作中,研究团队通过无穷镜将光束整形成相互非相干的一维虚拟光源阵列。通光定制的调制编码单元,每一个虚拟光源的光强度会以特定的频率随时间变化。这个经过时间调制的光源阵列通过光学元件形成单个光片后进入显微镜物镜并照射到荧光样品上。荧光成像沿用常规光片荧光显微镜的侧向采集方式。为了并行采集每层的图像,装置中人为引入球差增大成像焦深。这种设计提供了一种可行的方案克服了传统光片荧光显微镜由于机械扫描引起的稳定性差以及每层图像之间有时滞的瓶颈。同时,所采用的双反射镜设计有效地在相邻的兩束光之间引入时间延迟,使得照明的光片之间互不相干,减少在荧光成像中形成激光散斑,特别适合对散射介质中的结构进行成像。与传统的基于空间光调制或者激光分束的技术相比,采用双反射镜所生成的多光片具有光片数目以及相干性可控的优势。由于采用编码调制结合并行照明,可以实现对样品的深度结构进行低损伤成像,光损伤比传统的光片荧光显微镜更小。研究团队利用CLAM对含二氧化钛的人工散射介质中的荧光高分子微球进行成像,在300 μm穿透深度内仍能得到较好信噪比的图像。所构建的CLAM系统能对组织透明化的老鼠肾小球以及血管等重要组织结构进行三维成像。CLAM的应用还可以进一步拓展到发育生物学、细胞生长调控等研究,如对斑马鱼、果蝇等模式动物以及植物细胞的实时三维成像。在显微技术方面,非相干多片光照明以及编码调制技术可以方便的移植到传统的商用显微镜以及光片荧光显微镜上,实现多功能紧凑的光学显微成像系统。据悉,本论文的核心概念已提交了国际发明专利申请。
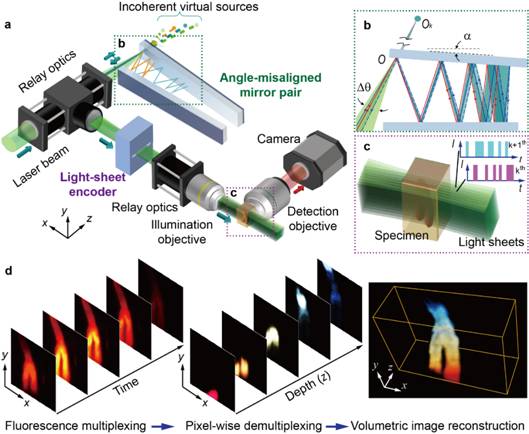
图1. 编码调制的光片荧光体成像显微镜(CLAM)原理示意图。
(a)所研制的显微镜原理示意图。准直的连续激光经柱透镜一维聚焦后进入双反射镜腔,一维光锥在腔内多次反射后在不同位置延原有路径折返。反射光等效于自一系列的虚拟光源发出,经调制单元调制后,每个虚拟光源的光强以特定频率随时间变化。虚拟光源可以经光学透镜转化成片状照明光并由物镜传递到样品上。荧光探测由侧向的成像系统完成。



